
2023年10月26日,清华大学药学院张从刚课题组在Immunity期刊发表了题为“SMPDL3A is a cGAMP-degrading enzyme induced by LXR-mediated lipid metabolism to restrict cGAS-STING DNA sensing”的研究论文。该研究发现肝X受体(liver X receptor, LXR)脂代谢通路的激动剂(T0901317等)能够诱导一种酶SMPDL3A的表达,该酶能够特异性地降解cGAS-STING信号通路的第二信使2’3’-cGAMP,从而特异性地抑制cGAS-STING天然免疫通路的激活。这是迄今为止首次发现能够靶向cGAMP降解的小分子抑制剂,从而为特异性地抑制cGAS-STING DNA免疫异常激活提供了新的思路,并且为相关的自身免疫性疾病、衰老以及神经炎症等众多疾病的治疗提供了重要靶点和新策略。
科研背景:
cGAS-STING信号通路是主要的DNA感应天然免疫信号通路。近几年,一系列的研究表明,机体的cGAS-cGAMP-STING通路能够被异常激活(比如被异常泄露的线粒体DNA激活),从而导致慢性炎症,在神经炎症反应、肾炎以及衰老等诸多疾病中起关键的驱动作用。所以开发特异性的cGAS-STING信号通路的抑制剂,对于相关的炎症疾病的治疗,具有重要的理论意义和潜在的临床应用价值。
另一方面,脂代谢信号通路被报道通过各种途径参与机体的免疫调控。其中,LXR脂代谢信号通路尤其引人注意,其激活被广泛报道能够抑制炎症反应,尤其在神经炎症领域,具有潜在的临床治疗潜力,但是相关的作用机制一直不太清楚。
科研成果:
该研究团队通过高通量的药物筛选平台发现小分子T0901317能够特异性地抑制2’3’-cGAMP激活的STING天然免疫应答,但是不抑制其他的STING激动剂(包括3’3’-cGAMP,c-di-GMP,c-di-AMP等环状核苷酸类激动剂;以及SR-717,DMXAA等非核苷酸激动剂)激活的STING天然免疫反应。这是首次发现一种小分子抑制剂,能够高效并且特异地靶向cGAS-STING DNA天然免疫的第二信使cGAMP,抑制cGAMP介导的天然免疫应答。
接着该团队深入探究这种特异性小分子抑制剂的靶点和作用机制。该团队假设,小分子T0901317可能诱导了一种2’3’-cGAMP特异性的降解酶的表达。为了验证这一假设,他们建立了一种cGAMP analog共价连接的探针,用此探针来钓取T0901317诱导的cGAMP结合蛋白。通过这种方法结合质谱技术,他们发现了一种酶SMPDL3A是特异性的2’3’-cGAMP降解酶。该团队证明,cGAS-cGAMP-STING通路的小分子抑制剂T0901317-----作为一种LXR脂代谢通路的激动剂,激活LXR信号,从而诱导cGAMP降解酶SMPDL3A的表达来抑制STING天然免疫反应。同时,该团队证明其他的LXR脂代谢通路的激动剂也有类似的抑制效果。
蛋白酶SMPDL3A是继ENPP1之后,在哺乳动物体系中发现的第二个2’3’-cGAMP降解酶。SMPDL3A本身就是一个分泌蛋白,它能够被LXR脂代谢信号通路诱导表达,特异性地抑制cGAS-STING免疫信号。所以LXR激动剂,以及SMPDL3A工程化蛋白,理论上有潜力治疗由cGAMP引起的异常炎症反应。该团队结合生化、细胞生物学、结构生物学和动物模型的技术方法,从体外、细胞到动物水平,证明了LXR-SMPDL3A module在cGAS-cGAMP-STING信号通路上的抑制作用。
综之,该研究揭示了一种新型的cGAS-STING信号通路的负调控机制,发现了一种新型的cGAMP降解酶。该研究扩大了我们对LXR脂代谢和cGAS-STING先天免疫调节网络的认识,这对于精准治疗神经炎症、衰老以及自身免疫性疾病具有重要科学价值和指导意义。
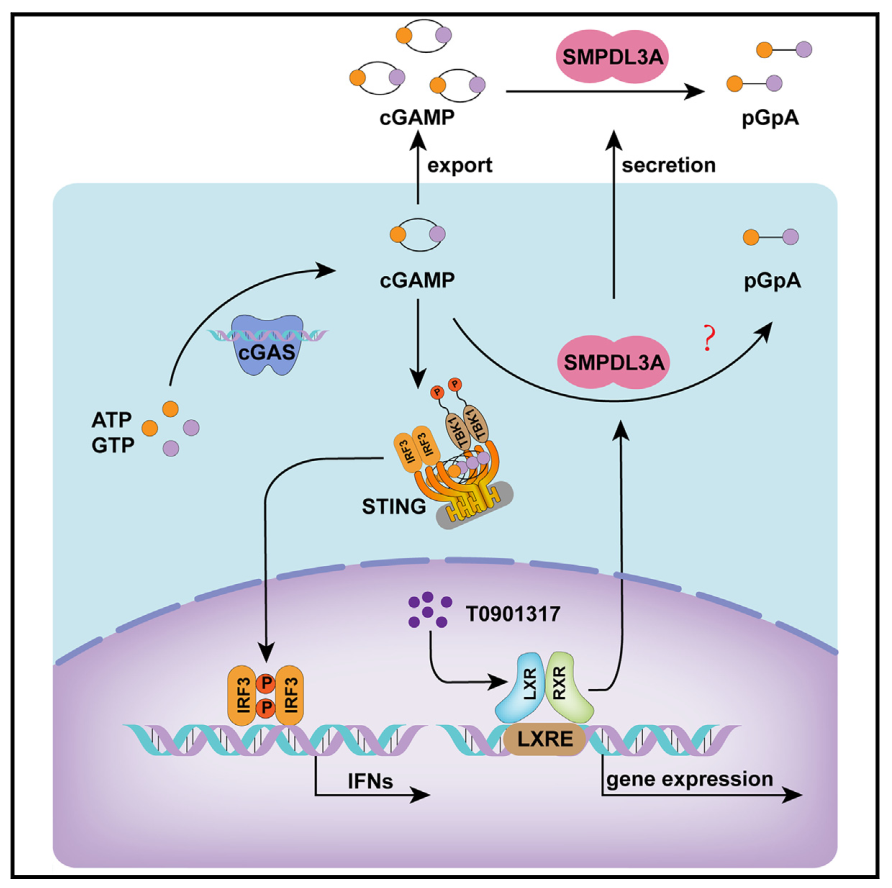
模式图. T0901317激活LXR脂代谢诱导SMPDL3A的表达,降解cGAMP来抑制cGAS-STING信号
清华大学药学院张从刚研究员为该论文通讯作者,张从刚课题组博士生侯燕飞、博士后王志萌、天津大学刘培源老师,中国农业大学卫旭彪老师(原实验室博士后)为该论文第一作者,清华大学X射线晶体学平台的范仕龙老师以及清华大学药学院的储凌老师在该课题实施过程中提供了宝贵的技术帮助,清华大学药学技术中心提供了平台技术支持。该研究得到了国家自然科学基金项目、清华-北大生命科学联合中心、北京市自然科学基金以及中国博士后科学基金的资助。
原文链接:https://doi.org/10.1016/j.immuni.2023.10.001


