4月6日,清华大学药学院陈立功课题组及其合作者在《Gut》 在线发表了题为《胆固醇生物合成支持由小鼠和人体内脂肪酸合成酶缺失引发的肝癌病变的继续生长》(Cholesterol biosynthesis supports the growth of hepatocarcinoma lesions depleted of fatty acid synthase in mice and humans)的研究论文,该研究首次发现胆固醇的累积可以支持由脂肪酸合成酶(Fatty Acid Synthase, Fasn)缺失引起的肝癌病变的继续生长,同时抑制脂肪酸和胆固醇的合成可以有效降低肝癌的发生。该课题综合利用肿瘤模型、代谢表型分析、基因组学分析、脂质组学分析、人类肝细胞癌模型和临床数据以及抗肿瘤联合用药等多种手段, 研究结果强烈建议同时瞄准脂肪酸从头生成和胆固醇生物合成可能是治疗和预防肝细胞癌的有效途径, 为肝细胞癌的发生发展机制和治疗靶点发现做出了非常重要的探索!
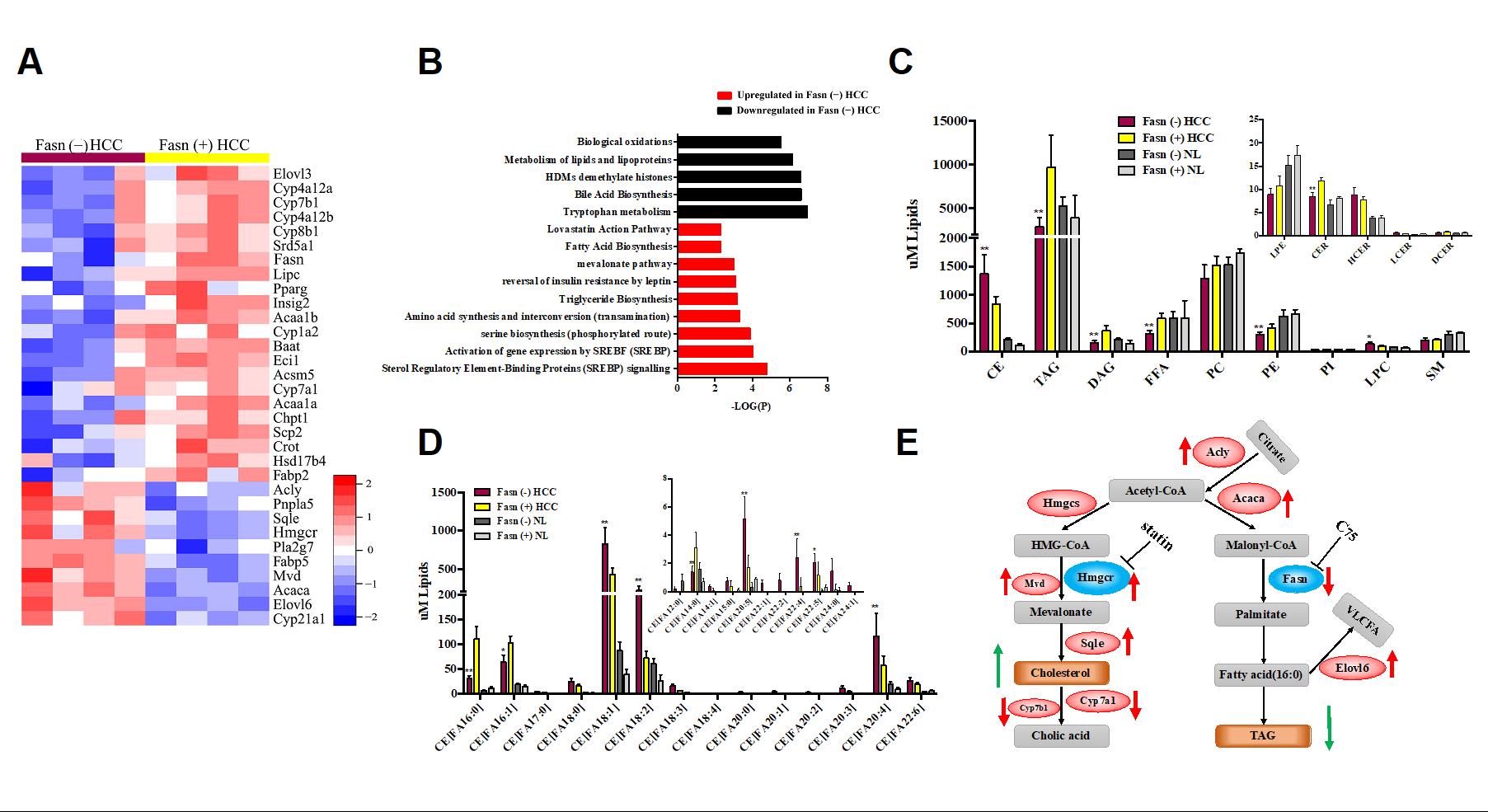
图1. Microarray和脂质组学分析
(A-B) Microarray数据分析 (C-D)脂质组学分析 (E)甘油三酯和胆固醇代谢调控总结
在过去的几十年里,原发性肝癌的全球发病率逐渐增加。原发性肝癌主要以肝细胞癌(Hepatocellular carcinoma, HCC)为主,并且治疗HCC的选择方案比较有限。目前治疗晚期HCC的标准药物主要是多重激酶抑制剂Sorafenib和Regorafenib,但它们的疗效又是有限的。因此,急需要找到治疗肝细胞癌的新药靶点。
为了满足快速增殖的需要,肿瘤细胞表现出不同与正常组织细胞的代谢特征。虽然癌症类型和病因各有不同,癌细胞中代谢通路的变化却有一定的相似性,葡萄糖代谢途径、磷酸戊糖途径和谷氨酰胺代谢途径都发生变化来适应癌细胞的快速生长和增殖。最近的研究表明,许多脂肪酸代谢途径在癌细胞中也发生了改变。在癌症发展过程中,脂肪酸代谢通路的变化不仅为癌症的发生和发展提供能量,还在生物膜大分子以及信号分子等方面扮演重要角色。肿瘤组织发生的脂肪酸代谢改变为其异常存活与生长提供能量和大分子的前体等,提示学者们针对关键的代谢临床动作会是十分有效的治疗方法。
在本篇研究中,陈立功课题组及其合作者以同时抑制Pten和过表达c-Met基因(sgPten/c-Met)诱导肝脏条件敲除脂肪酸合成酶Fasn小鼠来发生原发性肝癌为实验模型,通过Microarray和脂质组学分析揭示了,在肝癌组织中,脂肪酸合成酶的缺失会造成甘油三酯的降低以及胆固醇的上升,并且引起SREBP2代谢通路的显著上调,抑制SREBP2可以完全的阻止sgPten/c-Met诱导的肝脏条件敲除脂肪酸合成酶Fasn小鼠发生肝癌。同时在人类HCC细胞系中,敲除Fasn显著增加了SREBP2的入核和HMG-CoA 还原酶(HMG-CoA reductase, HMGCR)的表达,并且共同抑制Fasn介导的甘油三酯和HMGCR介导的胆固醇合成通路,导致人类HCC细胞系的凋亡。因此,共同抑制脂肪酸和胆固醇合成通路也许是治疗HCC的一个新的选择。
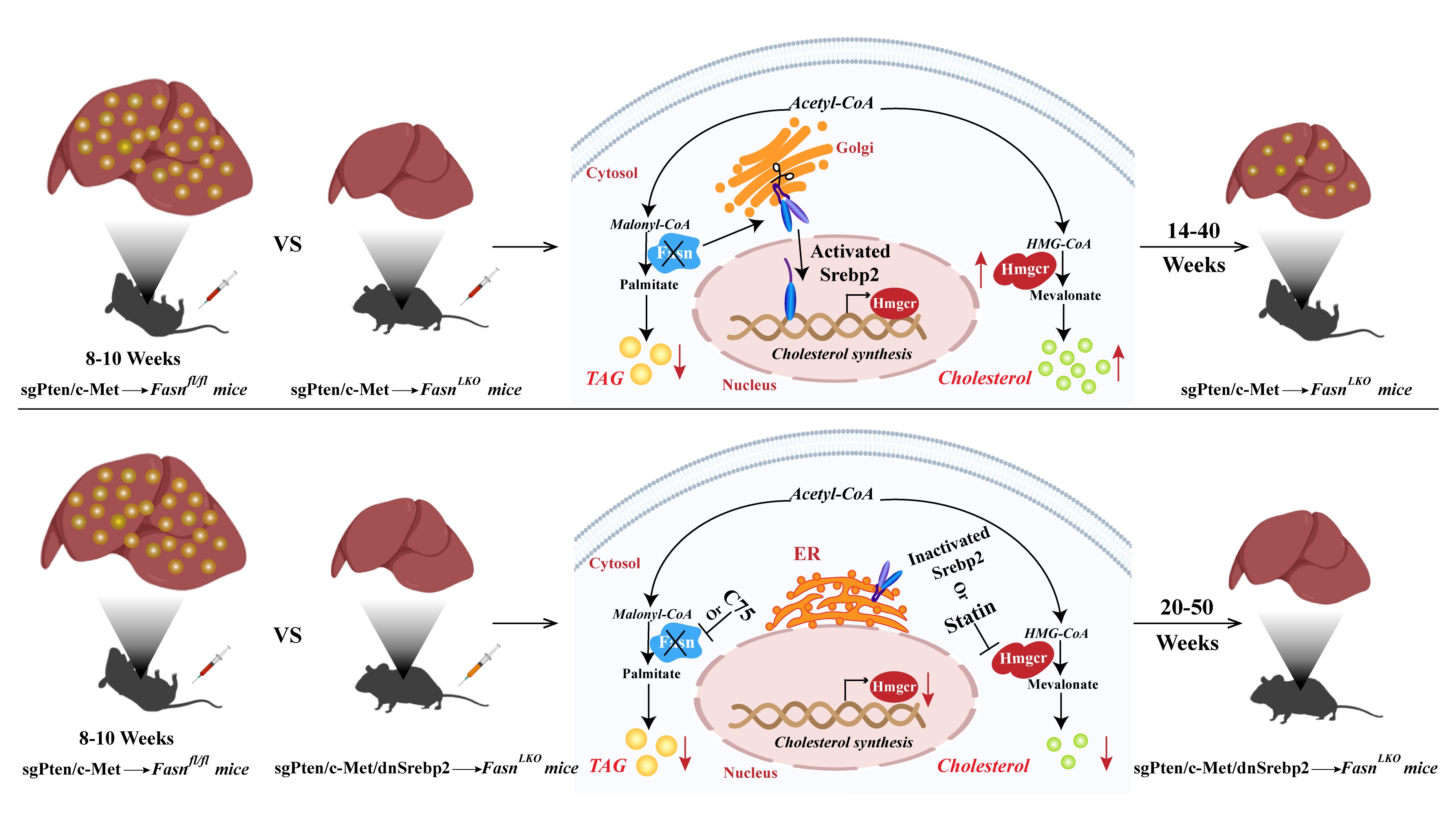
图2. 共同抑制脂肪酸和胆固醇合成阻止肝癌的发生
《Gut》是胃肠肝脏学科期刊中的顶尖杂志。 该论文核心通讯作者为清华大学药学院陈立功研究员, 旧金山加州大学 Xin Chen教授以及意大利萨萨里大学Diego F. Calvisi教授为共同通讯作者,药学院研究生池文娜、刘烨、马志龙和匡文华为本论文的重要合作作者,在脂质组学、机制分析和细胞模型建立上承担了重要的工作。同时,中国科学院遗传与发育生物学研究所税光厚课题组和北京大学张泽民课题组在脂质组学和人类肝癌数据分析提供了重要帮助。该研究得到了国家重点研发计划、国家重大新药创制项目以及国家自然科学基金委的资助。
文章链接:
https://gut.bmj.com/content/early/2019/04/05/gutjnl-2018-317581


