最新研究速递
2024年9月16日清华大学药学院蒯锐课题组在Nature Communications发表题为“Tuning the fluidity and protein corona of ultrasound-responsive liposomal nanovaccines to program T cell immunity in mice”的文章。该研究揭示了脂质体的流动性和表面蛋白冠对其脾脏靶向递送特性的影响,并基于该发现制备了能高效扩增抗原特异性T细胞的脂质纳米疫苗,建立了一种能够将T细胞高效募集到肿瘤组织并产生强大的抗肿瘤效应的方法。

研究过程
大量研究表明增加实体瘤内肿瘤抗原特异性T细胞数量可提高肿瘤治疗效果。虽然许多肿瘤疫苗通过靶向淋巴结能有效扩增肿瘤抗原特异性T细胞,但这些T细胞并不总是能够有效到达肿瘤,从而限制治疗效果。以往研究表明,使用肿瘤疫苗后在肿瘤组织局部注射趋化因子或Toll样受体激动剂可以促进抗原特异性T细胞向肿瘤组织的募集,但这一策略不适用于难以直接注射的肿瘤。理想的解决方案是设计一种疫苗使其不仅可以靶向淋巴器官激活大量的抗原特异性T细胞,同时还可以精准调控肿瘤微环境(如增加趋化因子或者粘附分子表达)以促进T细胞向肿瘤组织的募集。但目前能安全有效地实现这一目标的方法依然非常欠缺。
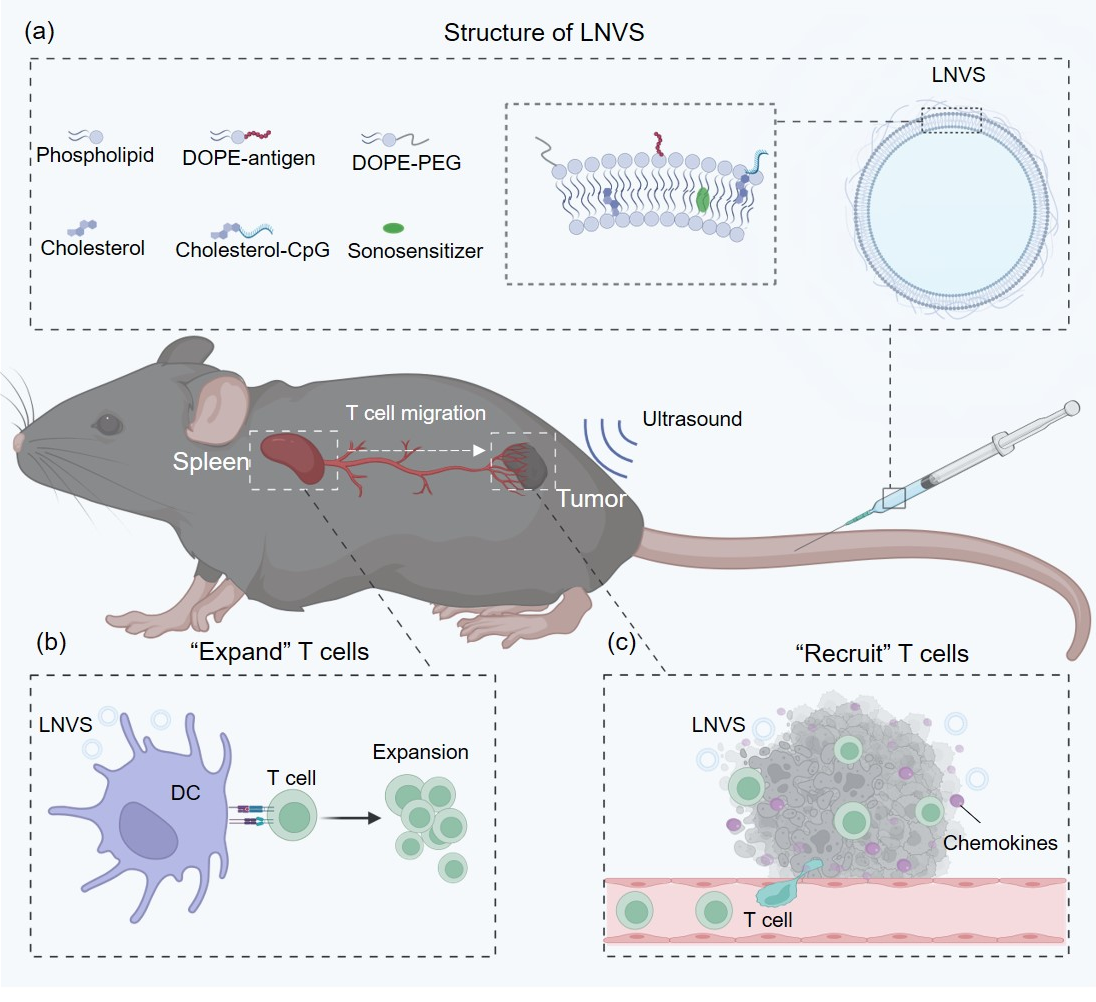
针对以上瓶颈问题,蒯锐课题组开发了一种具有超声波(Ultrasound,US)响应性的脂质纳米疫苗(Liposomal Nanovaccine containing a Sonosensitizer , LNVS)以同时控制T细胞的扩增及在肿瘤组织的募集。LNVS由脂质体载体、疏水修饰的肿瘤抗原和佐剂、声敏剂三个模块构成,其粒径约为150纳米。研究团队首先发现在健康小鼠上脂质体载体的高流动性以及富含补体C3的蛋白冠对其在脾脏的蓄积和激活T细胞应答至关重要,降低脂质膜的流动性或者敲除小鼠体内的补体C3均会显著抑制脂质体在脾脏的蓄积并降低抗原特异性T细胞应答。基于这些发现研究团队进一步构建了具有适宜流动性和蛋白冠的超声响应性脂质纳米疫苗LNVS。在小鼠肿瘤模型上,静脉注射的LNVS一方面能高效蓄积在脾脏扩增抗原特异性的T细胞;另一方面部分LNVS可被动蓄积在肿瘤组织,在肿瘤组织应用超声波可以激活声敏剂产生活性氧并显著增加肿瘤组织中趋化因子和黏附分子的表达,最终促进T细胞向肿瘤组织的募集。LNVS+US比传统的声动力疗法(Sonodynamic Therapy, SDT)或者普通脂质纳米疫苗诱导更高水平的肿瘤内抗原特异性T细胞,在多种小鼠肿瘤模型中均表现出优异的治疗效果,并能保护治愈的小鼠免于复发。清除循环系统中的T细胞显著削弱治疗效果,表明外周T细胞向肿瘤组织的募集对治疗效果有重要贡献。
研究结论
该研究报道了一种利用超声波响应性的脂质纳米疫苗LNVS控制T细胞的扩增和在肿瘤组织的募集的方法。静脉注射的LNVS以一种高度依赖脂质流动性和表面蛋白冠组成的方式在脾脏蓄积并扩增抗原特异性的T细胞。此外,部分LNVS可以被动蓄积在肿瘤组织,并响应超声波产生活性氧进而增加肿瘤组织中趋化因子和黏附分子的表达,最终促进抗原特异性T细胞向肿瘤组织的募集并产生强大的抗肿瘤效果。
致谢
清华大学药学院蒯锐研究员为本文的通讯作者。蒯锐课题组2020级博士生何嘉为本文的第一作者。蒯锐课题组已出站博士后王超钰、方笑,博士后李君耀、沈雪莹做出了重要贡献。清华大学生命科学院李赛教授、博士后张俊霞、博士生彭程及清华大学医学院博士生李泓健为本课题的开展提供了大量帮助。本课题得到了国家高层次人才计划青年项目、国家自然科学基金、清华-北大生命科学联合中心、清华大学前沿交叉专项、笃实专项等基金支持。
原文链接:https://www.nature.com/articles/s41467-024-52104-z


