2025年11月29日,由清华大学尹航教授团队牵头,联合海内外学者合作完成的综述文章《Unveiling Heterogeneity: Innovations and Challenges in Single-Vesicle Analysis for Clinical Translation》在细胞外囊泡领域权威期刊《Journal of Extracellular Vesicles》正式发表。该文系统梳理了单细胞外囊泡分析技术的最新进展与转化挑战,指出微流控、超分辨成像与人工智能等方法的融合,正推动该技术向癌症早期诊断、个性化治疗及精准药物递送方向快速发展。
细胞外囊泡是细胞分泌的纳米级载体,参与细胞间通信,其分子组成反映来源细胞的生理或病理状态。传统群体分析方法难以揭示细胞外囊泡的高度异质性,而单细胞外囊泡分析技术能够逐颗粒解析其表面标志物、核酸内容物和功能特性,为疾病机制研究和生物标志物发现提供了全新视角。
这篇综述重点总结和分析了以下技术方向的进展:
高通量单细胞外囊泡分离:基于微流控的开发实现了低样本量(∼20 μL)、高纯度细胞外囊泡捕获,有效去除非目标颗粒干扰;
多参数表型分析:纳米流式与超分辨显微等技术相结合,实现对单细胞外囊泡粒径、膜秩序、蛋白组成的同步解析;
单细胞外囊泡多组学:通过DNA条形码与液滴包裹技术,实现单颗粒水平上百种蛋白质的同时检测,极大拓展了对细胞外囊泡异质性的认知边界;
人工智能驱动的数据分析:利用深度学习算法对海量单细胞外囊泡图像与分子数据进行自动分类与模式识别,显著提升分类准确性与诊断预测能力。
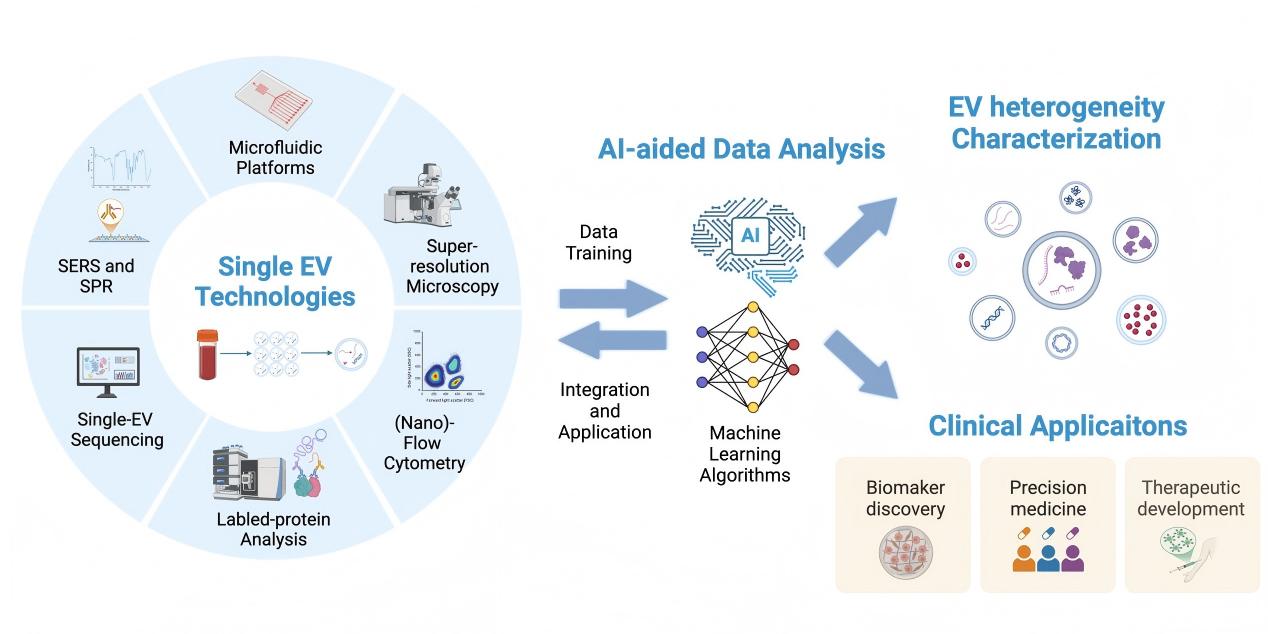
单细胞外囊泡分析在临床转化中展现出多层次价值:
1. 高灵敏度诊断:在乳腺癌、结直肠癌等模型中,成功实现基于表面蛋白与内部miRNA的单细胞外囊泡检测,准确区分早期患者与健康人群;
2. 治疗监测与个性化用药:动态分析患者循环中的细胞外囊泡亚群变化,可实时评估药物响应,为治疗策略调整提供依据;
3. 工程化细胞外囊泡作为递送系统:通过单颗粒水平载药量与靶向能力的量化,推动下一代细胞外囊泡药物的优化与标准化。
尽管技术快速进步,该领域仍面临分离标准化、检测通量、数据整合等挑战。未来,需要加强跨学科协作,建立统一技术规范,并推进多模态技术与AI模型的整合,以加速单细胞外囊泡分析从技术平台向临床工具的转变。
本综述的第一作者是清华大学药学院助理研究员张莹、博士后孟小童博士,以及澳大利亚贝克心脏与糖尿病研究所的David Greening教授。共同作者包括国内外多位深耕细胞外囊泡领域研究的专家。研究工作获得国家重点研发计划、国家自然科学基金及北京市自然科学基金等多个科研项目的支持。
原文链接:https://isevjournals.onlinelibrary.wiley.com/doi/10.1002/jev2.70209?sessionid=


