2025年11月25日清华大学药学院蒯锐/张从刚课题组合作在Nature Communications发表题为“Silencing PCSK9 reshapes the spatiotemporal activation of STING for safe and effective cancer immunotherapy”的文章。该研究发现了前蛋白转化酶枯草溶菌素9(PCSK9)这一胆固醇代谢的关键调控因子对cGAS-STING信号通路具有负调控作用,揭示了PCSK9通过竞争性阻断STING由内质网向高尔基体转运进而限制STING激活的分子机制,并基于PCSK9在肝脏中表达水平远高于肿瘤的组织分布特征设计了同时装载PCSK9 siRNA 与低剂量 STING 激动剂的脂质纳米制剂,证明了该制剂经系统给药后能增强肿瘤组织STING激活同时显著减少肝脏STING激活,从而同时解决STING激动剂在实际应用中面临的安全性与有效性问题。
cGAS–STING信号通路作为天然免疫系统的核心抗病毒防御机制,能够特异性识别胞质内异常存在的DNA(肿瘤或病毒来源), 启动I型干扰素免疫反应,进而激活适应性免疫应答,最终清除病毒或肿瘤细胞。遗憾的是,近些年多项STING激动剂相关临床试验均显示出抗肿瘤有效性不足以及不良反应严重等问题。尽管近年来人们开发出了多种药物递送系统向肿瘤组织的天然免疫细胞高效递送STING 激动剂,从一定程度上解决了有效性问题,但由于cGAS-STING信号通路中未知负调控因子的存在,STING激动剂单药疗法依然无法满足临床有效治疗的需求。此外,STING在各主要器官中均存在广泛表达,目前尚无有效手段能够完全避免经系统给药后STING 激动剂对正常组织(特别是肝脏)的脱靶激活,这一问题已导致大量临床严重不良反应事件发生。
为克服STING激动剂在临床试验中面临的有效性与安全性问题的双重挑战,研究人员首先对临床结肠癌样本的转录组学数据进行分析,发现PCSK9可能是cGAS-STING信号通路的关键负调控因子。细胞功能实验证实沉默或敲除PCSK9均可增强低剂量STING激动剂的免疫激活效应。分子机制研究表明,PCSK9对cGAS-STING信号通路的调控作用独立于胆固醇代谢水平变化以及其对膜蛋白的经典调控作用,而是与内质网货运受体蛋白SURF4相关。SURF4是调控COPII囊泡货物蛋白分拣的关键货运受体,广泛参与多种蛋白在内质网与高尔基体之间的顺向转运,这一过程同时也是PCSK9分泌与STING激活的限速环节。本研究发现SURF4是PCSK9与STING由内质网转运至高尔基体的共同货运受体,并且PCSK9对SURF4有更强的亲和力。这一亲和力的差异最终导致天然免疫细胞(树突状细胞或巨噬细胞)在免疫稳态/激活状态下PCSK9始终拥有更高的转运优先级,从而限制STING的持续/爆发式激活(图1)。由于PCSK9同时也是胆固醇代谢的重要调控元件,因此这一分子机制进一步加深了我们对胆固醇代谢与天然免疫信号通路之间独特调控模式的理解。
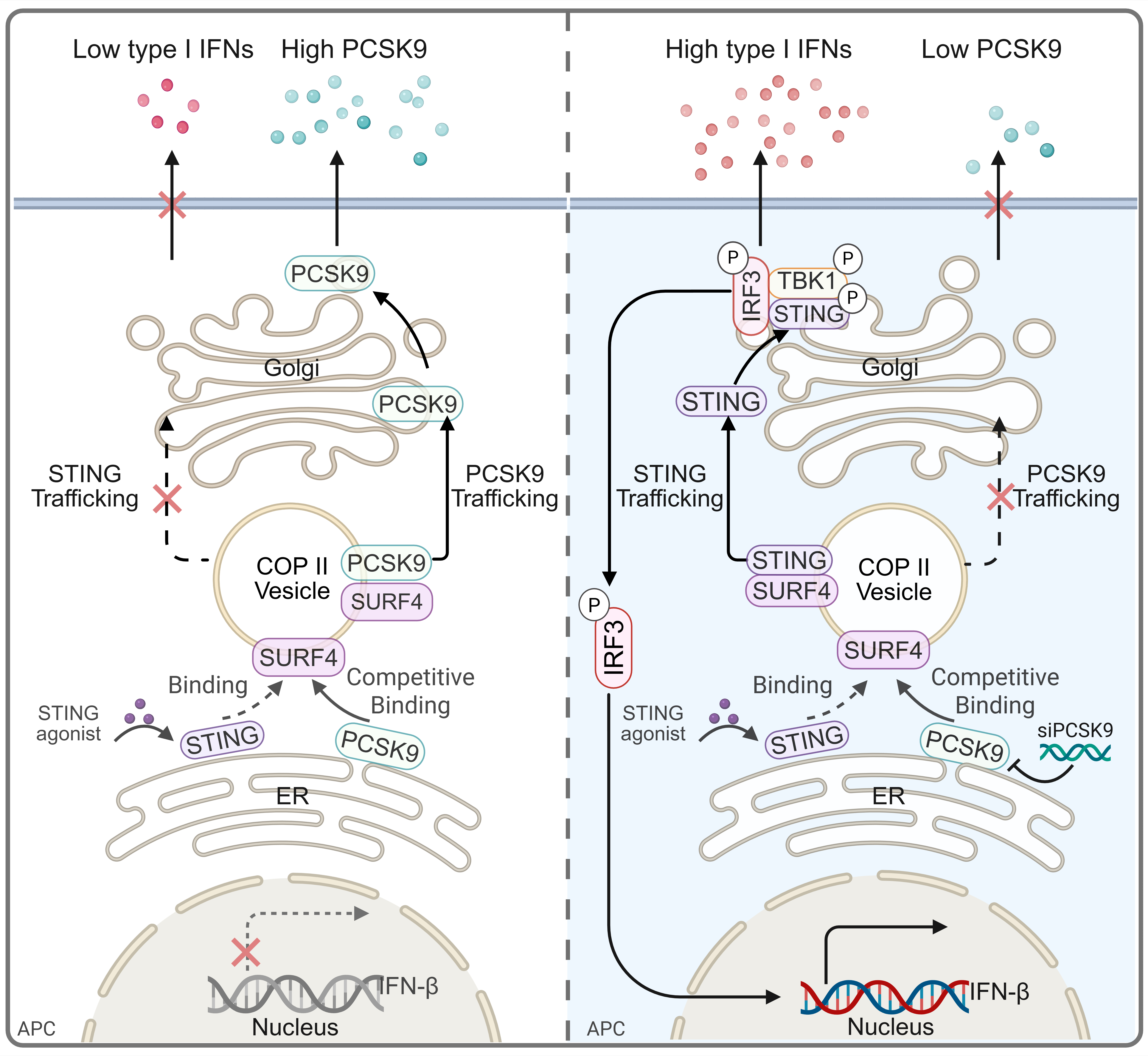
图1:PCSK9调控cGAS-STING信号通路的分子机制
值得注意的是,PCSK9是主要由肝细胞以及肝驻留免疫细胞表达的分泌蛋白,在组织层面有明显的肝脏高表达特征。因此,研究人员进一步设计了同时装载PCSK9 siRNA 与低剂量 STING 激动剂的脂质纳米颗粒,尽管该制剂在静脉给药后仍然在肝脏内观察到80%左右药物蓄积,但由于肝脏PCSK9表达水平远远高于外周或肿瘤浸润天然免疫细胞,这导致肝脏中PCSK9在基因沉默后仍有超过50%的蛋白表达,足以抑制肝脏STING激活产生的不良反应,而肿瘤中的PCSK9几乎实现完全的基因沉默,这导致肿瘤中的低剂量STING激动剂引起了强烈STING激活以及抗肿瘤免疫反应,最终实现了安全有效的免疫治疗(图2)。
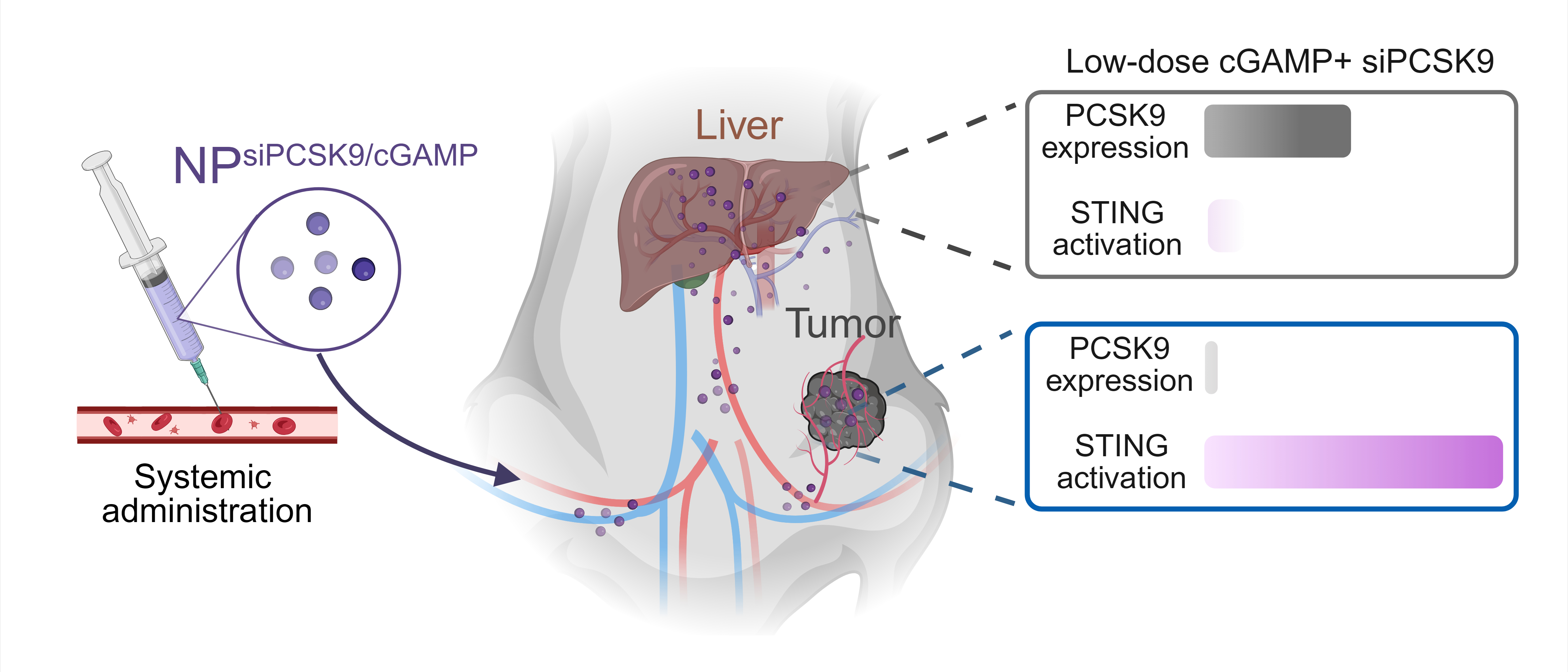
图2:含PCSK9 siRNA与低剂量STING激动剂的制剂调控STING时空激活特征示意图
本研究发现了PCSK9独立于胆固醇代谢调控作用的新功能,揭示了PCSK9对天然免疫系统进行“刹车”的分子机制,证明了靶向PCSK9可以重塑cGAS-STING信号通路的“时空”激活特性,在肿瘤部位强力激活免疫反应的同时,有效保护了肝脏这一重要代谢器官,为长期困扰STING激动剂临床试验的安全性与有效性难题提供了一种具有转化潜力的解决方案。
致谢
清华大学药学院蒯锐研究员,清华大学药学院张从刚研究员为本文的共同通讯作者。蒯锐课题组博士生孙鹏博,张从刚课题组博士生韩芳平为本文的共同第一作者。蒯锐课题组博士生吴程程,已毕业博士生李昕艳、何嘉,清华大学生命科学学院博士生邓婷月为本课题的开展提供了大量帮助。本课题得到了国家高层次人才计划青年项目、国家自然科学基金、清华-北大生命科学联合中心、清华大学前沿交叉专项、笃实专项等基金支持。
原文链接: https://www.nature.com/articles/s41467-025-66630-x


