2025年11月26日,清华大学肖百龙课题组在《细胞报告》在线发表了题为《机械门控PIEZO通道以一种弹簧样的力学机制实现快速失活和随机性的单通道门控》的研究长文,报道了PIEZO通道如何凭借一种“弹簧样”结构元件与力学机制,精准调控其快速激活与失活,并决定其随机性的单通道开放与关闭的电生理特性。此项工作不仅深化了对PIEZO通道工作机制的理解,而且提出了离子通道在单分子水平的“随机性”行为由其内在结构机制决定的新观点。

科研快讯
在微观的分子世界中,受热涨落驱动,每个分子都像拥有“自由意志”,表现出“随机性”的行为。离子通道通过响应化学配体或机械力等不同刺激,调控离子跨细胞膜的通透性。在单分子水平上,离子通道同样呈现“随机性”的开放与关闭行为,这一现象已通过膜片钳记录技术获得了近半个世纪的实验验证。然而,这种单通道的“随机性”行为是否由其内在的结构机制所决定,仍是未解之谜。
机械门控PIEZO离子通道是一类关键的机械力受体,能将机械力刺激转化为细胞的电化学信号。它们参与介导多种核心的生理过程,包括触觉、痛觉、本体觉、内脏觉(如呼吸、血压、膀胱充盈、肠道蠕动),以及心血管、大脑、骨等器官组织的功能稳态维持与调控。此外,PIEZO通道的功能异常与多种人类疾病密切相关。
在全细胞电生理记录模式下,PIEZO1通道能够快速响应机械力刺激并产生宏观电流(图1D,mPIEZO1蓝线部分),随后迅速衰减进入失活状态(图1D,mPIEZO1红线部分)。而在单通道水平,PIEZO1则表现出反复随机的开放与关闭行为(图1D,mPIEZO1左下)。值得注意的是,在持续机械力刺激下,这种单通道的开放与关闭行为持续存在且无明显失活,呈现典型的“随机性”单分子行为。
本研究综合运用结构分析、定点突变载体构建、膜片钳电生理记录以及分子动力学模拟等多种技术手段,系统揭示了PIEZO通道胞外帽状结构的连接器(linker)作为一种熵弹簧,决定其上述典型电生理特性的力学机制。
肖百龙团队与合作者多年来系统解析了PIEZO蛋白在不同构象下的高分辨率结构。本研究首先基于已报道的PIEZO1的关闭态、中间开放态和失活态结构,发现连接胞外帽状结构与成孔跨膜区的两段连接器——OC-linker和S-linker——在PIEZO1通道的门控过程中表现出显著的、类似弹簧往复运动般的伸缩变化,同时伴随着帽状结构闸门(cap gate)与跨膜闸门(TM gate)的开放与关闭(图1A-1C)。这一动态结构特征提示,OC-linker和S-linker可能以类似弹簧的力学机制参与通道门控。
研究者进一步利用果蝇PIEZO通道与小鼠PIEZO1通道在电生理性质上的显著差异(图1D,dPIEZO),构建了二者连接器互换的嵌合体载体。实验发现,连接器的互换导致了相应电生理特性的互换。通过系统性的定点突变及电生理功能验证,研究确定了OC-linker两端的特定氨基酸残基(I2213和D2225)以及S-linker上的S-helix结构和G2465铰链位点共同参与调控通道的失活与激活过程(图1D)。
通过引导分子动力学模拟(steered molecular dynamics, SMD)、计算及结构分析,研究者发现OC-linker和S-linker在门控过程中表现出熵弹簧的特性。定量分析表明,3对OC-linker和S-linker在门控过程中所需的总能量约为4.8 kBT,接近环境热能的量级。
为了更精细地解析连接器对PIEZO通道门控的影响,研究者在单通道水平上观测了上述关键位点突变体的电生理特性。有趣的是,PIEZO通道的单通道开放时长与其宏观电流的失活时间呈线性相关。所有记录的单通道均表现出重复随机的开放和关闭行为,并且失活较快的通道变体其单通道开放频率显著高于失活较慢的PIEZO1通道(图1D,下部)。基于单通道开放概率计算得到的PIEZO1门控能量约为4.1 kBT,与分子动力学模拟所得到的4.8 kBT高度接近,进一步支持了熵弹簧模型的有效性。
综上,本研究提出了PIEZO通道失活和随机单通道门控的弹簧样力学作用机制。该机制的核心在于,OC-linker和S-linker作为熵弹簧,位于通道顶部的帽状结构与跨膜孔道之间。当机械力使帽状结构下移、桨叶区展平时,连接器从伸展的高熵状态转换为压缩的低熵状态,储存弹性势能,从而打开孔道,引发通道激活;随后,被压缩的连接器倾向于恢复其伸展状态,将帽状结构推回,促使帽状结构闸门关闭,通道快速失活。而在环境热力学扰动下,处于上移状态的帽状结构和伸展的连接器能再次下移和压缩,重新打开帽状结构闸门,使通道再次开放。这种弹簧式的压缩-释放机制使通道在稳态张力和环境热能作用下能实现可重复的开启-关闭循环,并决定了其随机而可控的单通道开关特性(图1A,1B)。
该研究揭示的PIEZO通道基于“弹簧样”连接器的力学机制可能普遍适用于多种离子通道的门控过程。研究者进而提出新观点,认为离子通道在单分子水平的“随机性”开放与关闭行为是由其内在结构机制所决定的。
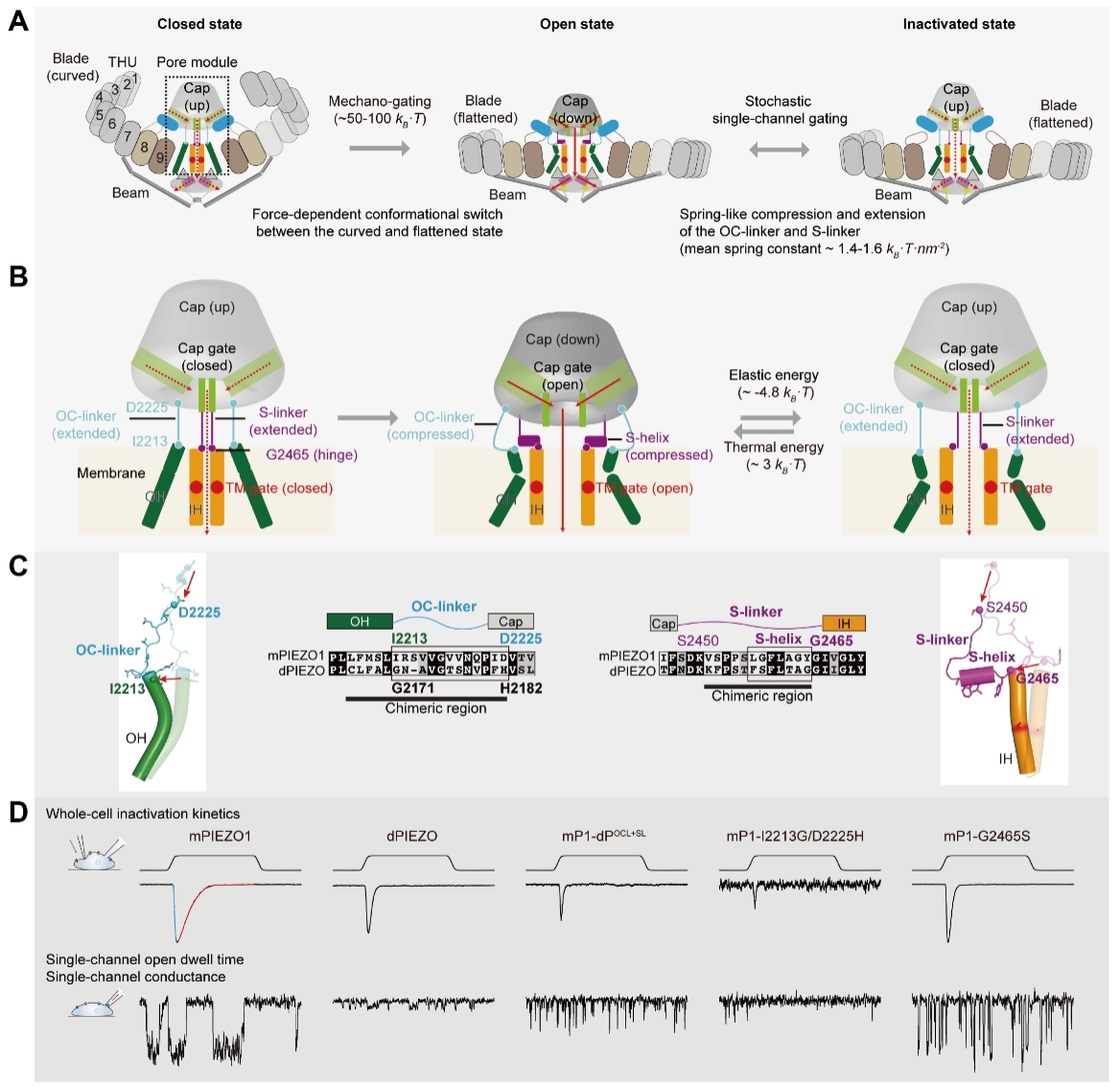
图1. PIEZO通道门控过程、弹簧样门控机制、连接器结构序列和电生理性质


