免疫系统如何“读懂”代谢变化?这一问题,正成为当代免疫学与代谢生物学交叉领域——免疫代谢(immunometabolism)——最核心的科学命题之一。近日,清华大学药学院张永辉团队联合多家单位,在《Nature》发表研究成果,系统揭示了甲羟戊酸通路关键中间体法尼基焦磷酸(FPP)在皮肤中的内源性免疫警报功能,并解析其调控全身体液免疫的分子机制。

类异戊二烯(isoprenoid)生物合成通路是地球上最古老、最保守的代谢网络之一。其化学基础源于两个小分子:异戊烯焦磷酸(IPP)和二甲基烯丙基焦磷酸(DMAPP)。在真核细胞中,它们通过甲羟戊酸(mevalonate)途径生成,并进一步转化为15碳的法尼基焦磷酸(FPP)和20碳的香叶基香叶基焦磷酸(GGPP),最终参与胆固醇及多种关键生物分子的合成。20世纪以来,Konrad Emil Bloch、Michael S. Brown和Joseph L. Goldstein等科学家系统阐明了胆固醇生物合成及其负反馈调控机制,奠定了现代脂质代谢研究的基础。随着研究深入,科学界逐渐认识到,甲羟戊酸通路不仅是胆固醇合成的“生产线”,更是一个动态可塑的代谢枢纽。在感染、炎症或细胞应激状态下,其代谢流量迅速重塑,并可能深度参与免疫系统调控。张永辉团队长期聚焦这一通路的免疫功能,提出:在漫长进化过程中,甲羟戊酸通路的代谢中间体可能构成一套“内源性免疫感知系统”。
在病毒感染或肿瘤早期,靶细胞内IPP与DMAPP异常积累,可被人体数量最多的γδ T细胞亚群直接识别,迅速触发免疫监视反应。张永辉团队及合作者在Immunity(2019)、Nature(2023)和Immunity(2025)等发表系列研究,系统解析γδ T细胞受体对代谢产物的构象识别机制,从代谢层面解释了其突破经典抗原呈递模式的分子基础。
如果说IPP/DMAPP代表“代谢警报”的激活端,那么其下游的GGPP则体现出抑制与调控的一面。2018年,张永辉课题组在Cell发表研究,首次揭示树突状细胞内GGPP通过参与小G蛋白异戊二烯化修饰,调控内体运输与抗原加工过程,影响CD4⁺ T细胞活化效率。这一发现明确了GGPP在固有免疫与适应性免疫衔接中的枢纽地位。在这一激活与抑制的两端之间,FPP的功能长期未被清晰界定。
FPP是IPP/DMAPP与GGPP之间的15碳中间体,同时也是胆固醇合成的重要原料,是代谢流量分配的核心节点。在探索代谢分子的免疫调节功能过程中,研究团队发现FPP具有疫苗佐剂样作用,可增强抗体生成。一次关键实验中,FPP注射至小鼠足垫后,局部皮肤出现角化异常和明显增厚。张永辉团队发现其表型与由TRPV3持续活化所致的Olmsted syndrome高度相似。这一现象提示,FPP可能通过调控角质形成细胞中的TRPV3通道,引发皮肤炎症反应。随后,张永辉团队通过化学合成、生物物理分析与计算模拟证实:FPP(而非IPP或GGPP)能够特异性结合TRPV3,建立了其分子作用基础。这一“意外发现”成为揭示新型皮肤免疫机制的突破口。基于此,张永辉团队提出,皮肤感染过程可能会导致FPP累积从而诱导TRPV3的活化,启动全身体液免疫。
随后,合作者清华大学生命学院刘万里教授与中国医学科学院皮肤病医院陆前进教授团队开展了长期、系统的研究,明确鉴定出FPP是来源于角质层细胞的内源性免疫警报素,并深入揭示了其调控全身性体液免疫的关键分子机制——即FPP-TRPV3-IL-6/CCL20-GC信号轴。为探索该机制的临床意义,合作团队重点关注了系统性红斑狼疮(SLE)这一经典自身免疫性疾病。通过对SLE患者皮肤病变组织进行单细胞RNA测序分析,研究发现患者角质形成细胞中,特别是TRPV3高表达的亚群,其UPR-甲羟戊酸通路异常激活,FPP-TRPV3-IL-6/CCL20信号轴处于过度活化状态,且该通路的活化程度与皮肤狼疮疾病活动度评分呈正相关。进一步的动物实验表明,金黄色葡萄球菌的定植可通过激活该信号轴加重狼疮模型小鼠的病理表现;而外源性FPP处理则显著提升抗dsDNA自身抗体滴度及尿蛋白水平,加剧肾脏损伤。相反,角质层细胞特异性敲除TRPV3可有效缓解FPP介导的狼疮病情恶化,进一步验证了该信号轴在疾病进展中的关键作用。这一发现不仅为“局部感染如何诱发系统性自身免疫”提供了分子机制解释,也为系统性红斑狼疮等疾病带来了新的干预思路。TRPV3及其下游炎症通路,可能成为未来治疗策略的重要靶点。
从阐明IPP和DMAPP被γδ T细胞识别的分子机制,到GGPP调控抗原呈递与免疫稳态,再到此次揭示FPP在皮肤中作为内源性警报分子的作用,张永辉团队围绕甲羟戊酸通路持续十余年的系统研究,逐步勾勒出这一古老代谢网络与免疫系统之间的深层联系。这些工作共同表明,甲羟戊酸通路并非单纯的胆固醇合成途径,而是贯穿先天免疫与适应性免疫、连接局部屏障组织与系统性免疫反应的关键代谢枢纽。代谢流量的变化,不再只是细胞内的生化调节过程,而可能构成机体感知感染与应激状态的重要信号基础。这一系列研究,为理解免疫系统如何“读取”代谢状态提供了新的理论框架,也为免疫相关疾病的干预策略奠定了坚实的代谢学基础。
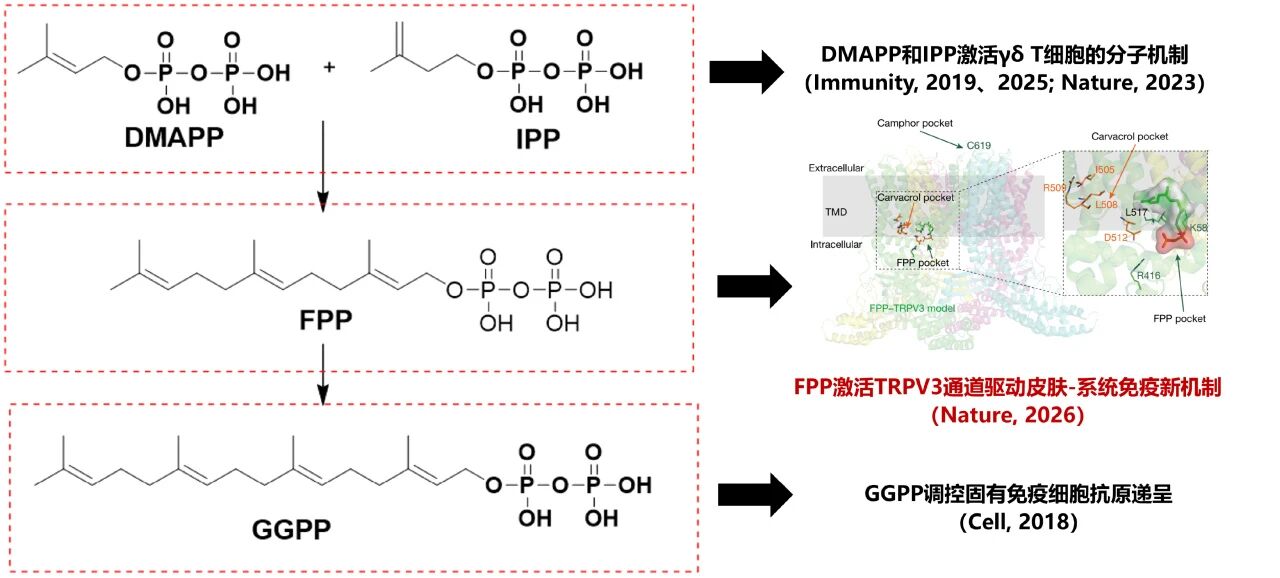
永辉课题组关于甲羟戊酸通路免疫调控的系列研究
清华大学生命学院刘万里教授,中国医学科学院皮肤病医院陆前进教授,清华大学药学院张永辉教授为共同通讯作者。药学院马先强博士为共同第一作者之一,张永辉课题组周晓英、赵乾程、夏赟等为本项目做出了重要贡献。
原文链接:https://www.nature.com/articles/s41586-026-10167-6?sessionid=


