最新科研速递
清华大学药学院尹航教授团队在《Biochemistry》特刊“Chemistry and Biology of Peptides”上发表了题为《Chemical Biology Drives Membrane-Curvature-Sensing Peptide Probes for Extracellular Vesicle Capture and Applications》的封面文章。该综述系统总结了团队在膜曲率感应多肽探针设计、改造与应用方面的系列工作,提出了一种基于EVs膜高曲率物理特性的捕获新范式,为EVs研究提供了从基础感知到转化应用的化学生物学工具平台。封面灵感源于作者作为医药学院足球队守门员在扑救来球时,需要合适的手型才能准确的拿到足球,同样地,多肽探针需要合适的曲率才能捕获对应大小的EVs。

图1 《Biochemistry》封面图
细胞外囊泡(EVs)作为细胞间通讯的关键载体,在疾病诊断、免疫调控与药物递送中展现出巨大潜力。然而,EVs不同的大小、来源、表面蛋白导致的异质性使得精准分离与捕获特定EV亚群成为技术瓶颈。因此,亟需发展一种不依赖于蛋白标记、能靶向EVs本质物理特性的新型捕获策略。尹航教授长期从事膜生物学、化学生物学的交叉研究,在细胞外囊泡与膜相互作用探针领域取得了一系列突破性进展,典型的EV多肽探针如MARCKS-ED,由尹航团队从天然膜曲率感应蛋白结构域(如BAR、ENTH结构域)中获得灵感,并通过化学生物学的手段设计合成了一系列具有膜锚定与曲率感应能力的短肽。本综述系统性地总结了针对EV的多肽分离探针特点和化学生物学改造方式,使得对EV的分离纯化策略不再通过物理手段,或EV的表面蛋白进行纯化,而是转向靶向EV膜本身固有的、保守的膜曲率和特征脂质。尤其对于外泌体等小尺寸EVs(30-150 nm),其膜的高曲率是一个稳定且普适的特征。利用化学生物学手段设计能够感知这一物理特性的肽探针,为EV研究提供了一种不依赖于蛋白标记、更接近其物理本质的全新工具。
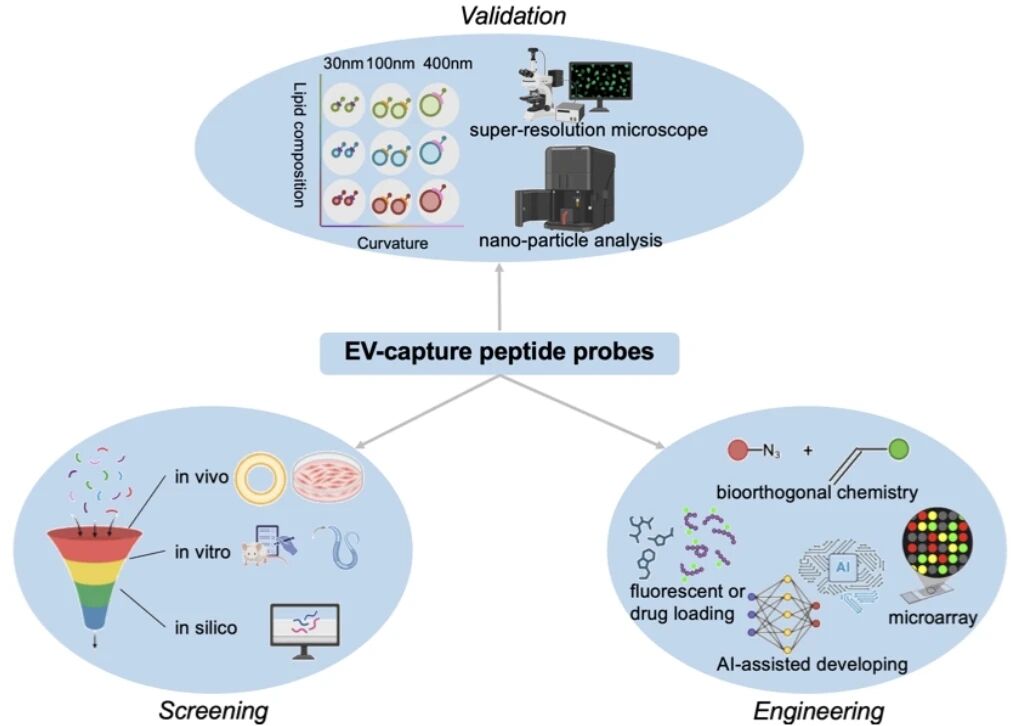
图2. 细胞外囊泡多肽探针的筛选、改造、验证策略
传统方法依赖超速离心、免疫亲和捕获等,或面临回收率低、纯度不足的问题,或受限于表面蛋白表达异质性,难以实现EVs的全谱系捕获与功能解析。相较于抗体、适体等传统探针,基于肽的膜曲率传感器展现出多种优势,包括成本、改造方式、稳定性等,总结如下:
1. 可通过固相肽合成快速、大规模制备,易于进行化学修饰,成本远低于抗体。
2. 氨基酸序列清晰,可精确调控其电荷、疏水性、构象,实现功能的理性设计。
3. 作为外源添加的探针,无需对细胞或EVs进行基因工程改造,可直接用于临床样本(如血浆、尿液)。
4. 采用D-型氨基酸修饰的多肽探针具有低免疫原性,高生物相容性和稳定性。
5. 能够捕获所有具有高曲率膜结构的EVs,克服了因表面蛋白异质性导致的捕获异质性,为研究EV全谱提供了可能。
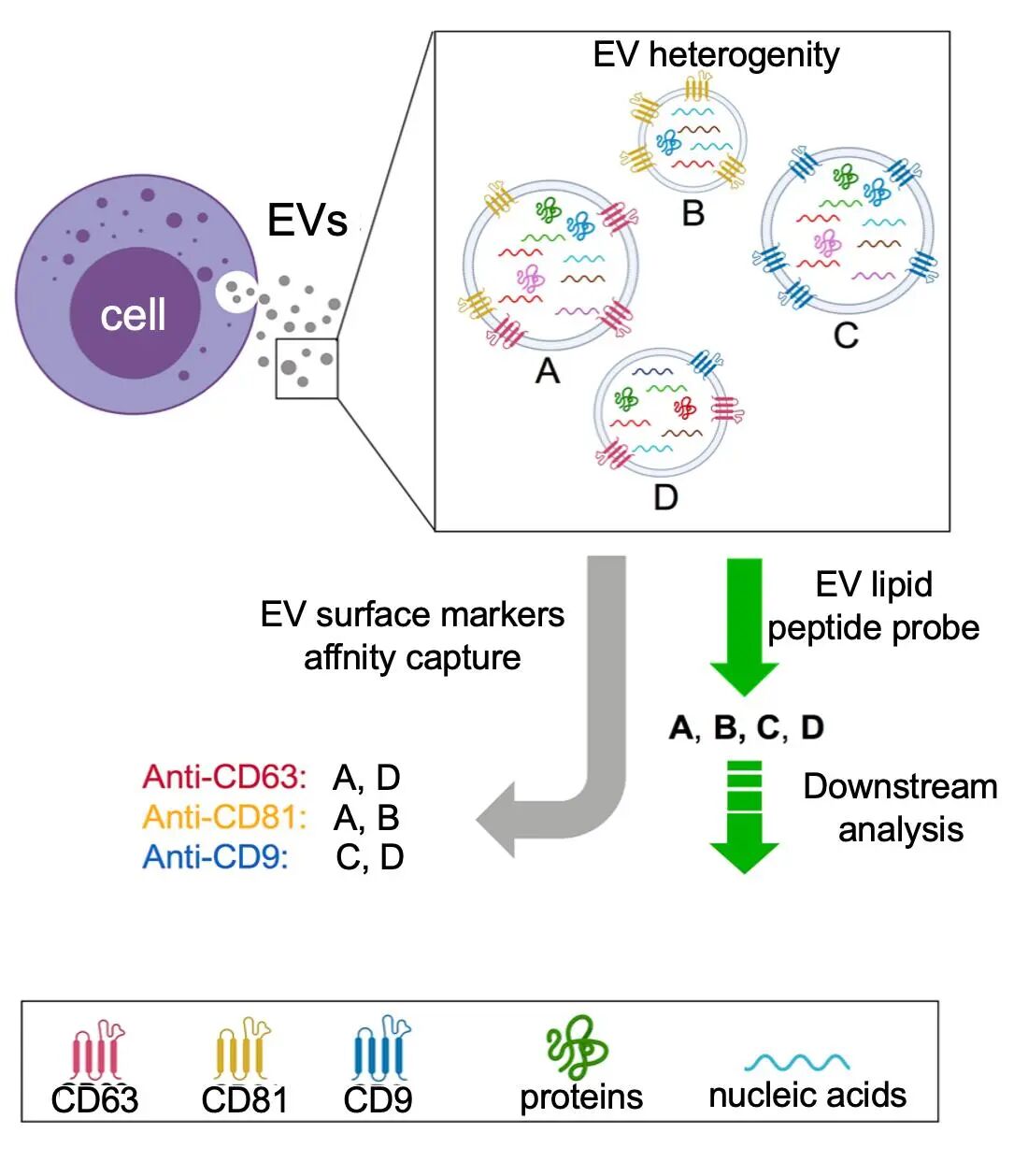
图3. 如针对EV的表面蛋白进行免疫捕获,会因为EV的异质性得到不同的亚群,难以合理的对EV进行富集。针对膜的多肽探针捕获策略可以从另一个维度纵向富集E
在本综述中,针对EV多肽探针的工程化改造,提出了一系列化学生物学生物正交策略,使多肽探针升级为具备实际应用潜力的强大工具,综述提供了四种化学生物学修饰改造的策略:
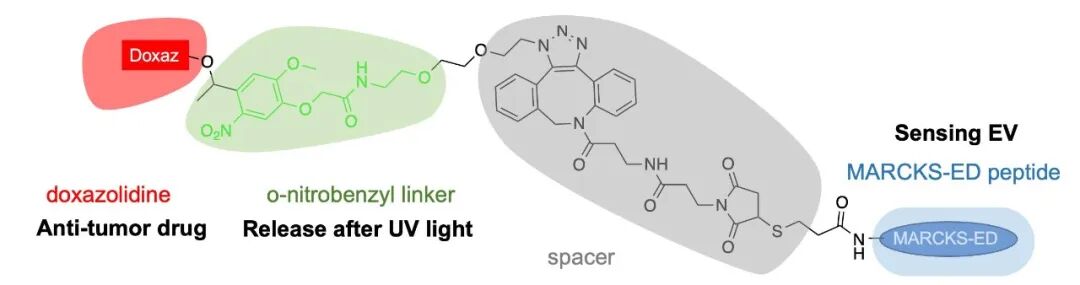
图4. 多肽探针的多种化学生物学改造方式(A)分子内点击化学环化反应、(B)分子间点击化学多聚反应、(C)多肽探针偶联光敏基团和药物分子
1. 通过氨基酸突变,研究多肽与EV的互作情况,并替换天然的L-型氨基酸,设计全D-型氨基酸多肽探针,在完全保留其膜曲率感知功能的同时,使其在生物体中的半衰期延长,为体内应用奠定基础。
2. 受天然蛋白多价相互作用的启发,利用点击化学将缓激肽衍生肽构建成三聚体,使其对EVs的结合亲和力提升了5倍以上,实现化学修饰获得更好的捕获探针转化。
3. 通过分子内环化策略,将来源于突触结合蛋白C2B结构域的线性肽通过分子内点击化学反应环化,显著提高了其结合力与曲率选择性。
4. 在肽序列中偶联生物正交反应基团(如叠氮、炔基),实现了与荧光基团、亲和标签或固体载体的精准、高效耦联,并用于体内靶向递送药物,构建用于成像、捕获、药物负载的多功能探针。团队构建光激活的MARCKS-ED-Photodox。该前药利用肽的EV靶向能力,富集于肿瘤微环境;在近紫外光照射下,可控释放活性药物分子。这首次实现了利用曲率感知肽进行时空可控的靶向化疗,为癌症治疗提供了新策略。
结合当下技术热点,对多肽探针的转化与应用前景进行了展望:
1. 功能化肽探针可用于修饰微流控芯片或捕获柱,实现从微量临床样本中自动化、高通量富集高曲率EVs,为液体活检提供新型、高效的EV捕获技术。
2. AI驱动的理性设计:结合分子动力学模拟产生的大数据与机器学习,建立肽序列-膜曲率敏感性预测模型,实现逆向设计具有预定性能的下一代探针。
3. 未来探针将融合曲率感知与特定脂质/糖链识别,不仅能区分大小,还能解析EVs的生物发生来源(如外泌体vs微泡),实现真正的功能亚型分选。
4. 推动从实验室规模的肽合成向符合药品生产质量管理规范(GMP)的规模化生产工艺迈进,并开发集成化的床边诊断设备,最终将这一源于基础生物物理洞察的技术,转化为惠及患者的诊断与治疗方案。
这篇综述总结了运用化学生物学工具改造的一系列多肽EV探针。从感知物理特性出发,到实现精准生物识别与调控,这些工程化肽探针正在架起一座连接基础膜生物物理与临床转化医学的桥梁,为未来生命科学的研究与疾病诊疗带来了无限想象空间。
本文章由清华大学药学院博士后孙高歌与尹航教授共同完成。该工作得到国家自然科学基金、国家重点研发计划等项目的支持。
原文链接:https://pubs.acs.org/doi/10.1021/acs.biochem.5c00700?sessionid=


